更新时间:2024-09-25 浏览次数:723
药品生产的安全性在GMP中提出了严格的要求,而作为洁净环境监测,浮游菌采样又是其非常重要的一环,2019年,磐麦科技与全球首台便携采样仪制造品牌Orum签署中国战略合作协议,能够给广大客户提供各种应用场景下浮游菌采样的解决方案。
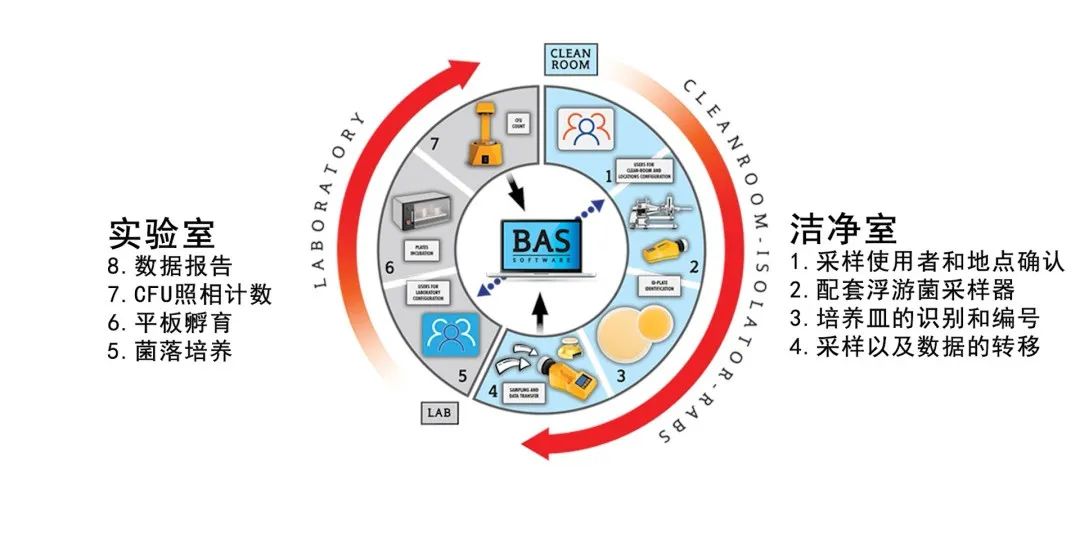
单头、双头、三头、压缩气体、隔离器等所有类型的浮游菌采样仪都能接入BAS数据管理系统,在不改变法规要求的采样流程下,真正做到了无纸化管理,让用户方便,省时,省力。 1.采样使用者和地点安排
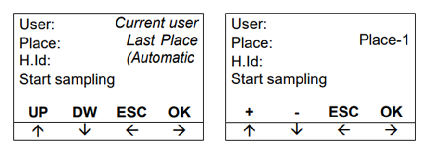
严格遵循GMP准则,可以通过软件提前预录地点和采样人名,无需用纸记录,极大地减少了人为操作带来的风险,保证数据的一致性。 2.配套浮游菌采样器
遵循ISO14698原则,采样速率可由100L/min升级到200L/min的采样器,一般情况下,A/B级区间采样时间为10mins,C级区间采样时间为5mins,对于洁净区间多的用户,在符合法规情况下,可以显著提高采样效率。 3.培养皿的识别和编号
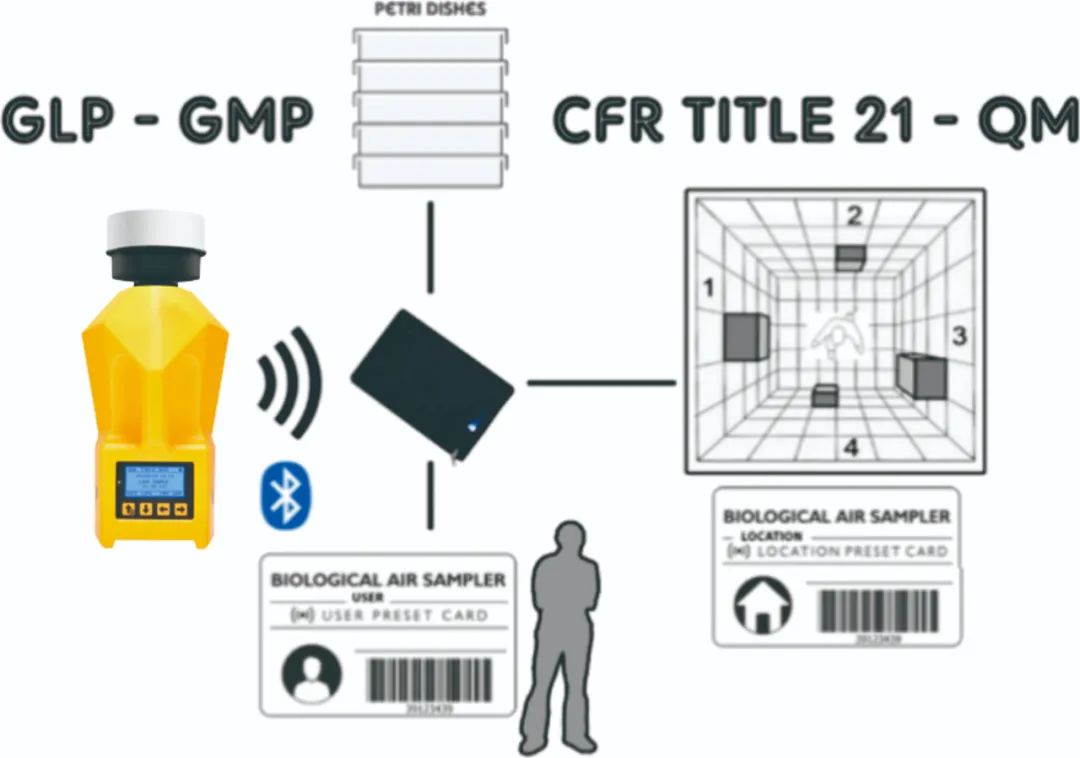
电子记录和电子签名符合ISO14698和FDA-21CFR-PART 11 原则,可通过蓝牙扫码器,对培养皿的信息通过扫码预录入仪器和适配软件系统,无需人手纸质记录。保证了数据的一致性,无纸化,也极大地减少了工作量,降低人为操作风险。 4.采样以及数据的转移
仪器内部自带记忆功能芯片,能存储1000个数据。连接后,仪器数据和管理软件系统保持一致,并且管理软件内部记忆数据录没有限制,同样符合FDA-21CFR-PART 11 和数据一致性原则。 5-6.菌落培养和平板孵育
符合ISO14698原则,同时BAS系统可以直接上传操作人员信息和数据数量,也可上传培养箱信息,无需手动用纸记录,方便内部人员信息对接,保证数据的一致性,也方便整体报告输出。 7-8:CFU照相机及数据报告
所有报告以及采样信息均被BAS数据管理系统记录并可导出,CFU照相系统匹配BAS管理数据库可上传照片。
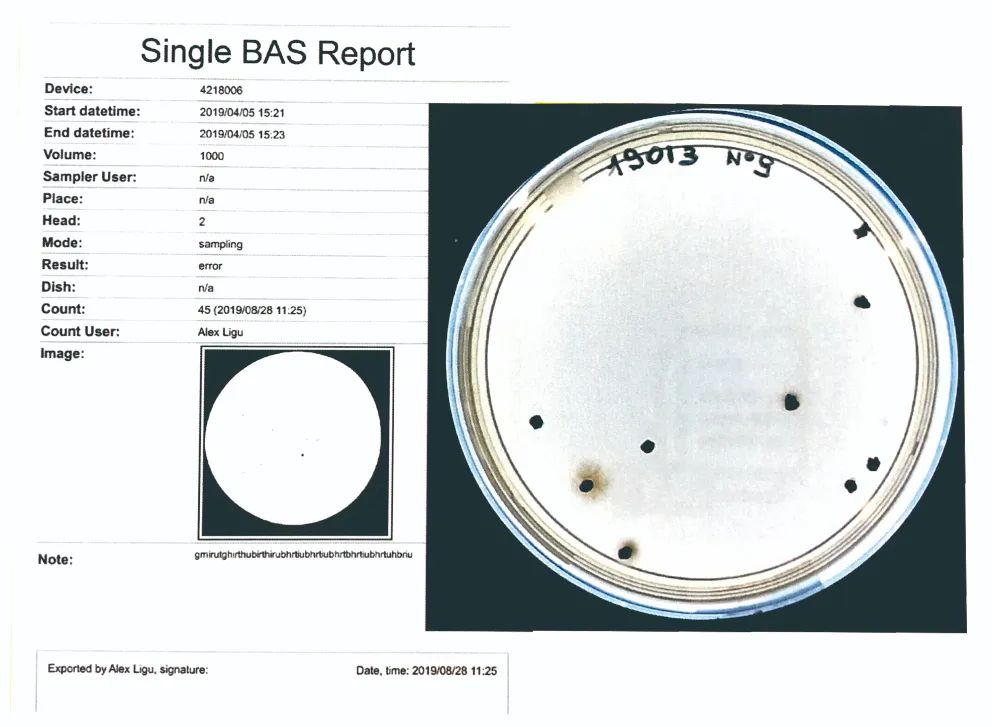
报告分为总表与单个报告,包含内容全面:时间,地点,采样人,开始/结束时间,培养皿编号,仪器编号,菌落计数,采样速率,仪器模式等,可以直接打印签名留档,还可根据总表点击查询单个培养皿报告细节,导出为PDF格式文档(不可修改)。
该过程全程使用电子记录和电子签名,不仅符合21CFR-PART 11 原则,而且符合数据一致性、数据不可修改、数据可溯源性原则,无纸化管理,录入数据全面,方便后期人员管理备案。 9:为下一次采样做准备
采样器使用全防护型机身,采用抗菌涂层的高强度树脂材料制造,不仅轻便,而且可直接在洁净车间VHP熏蒸,无需酒精擦拭消毒,避免使用一次性消毒袋,节约时间和成本,简化消毒流程。